肾结石(专业版)
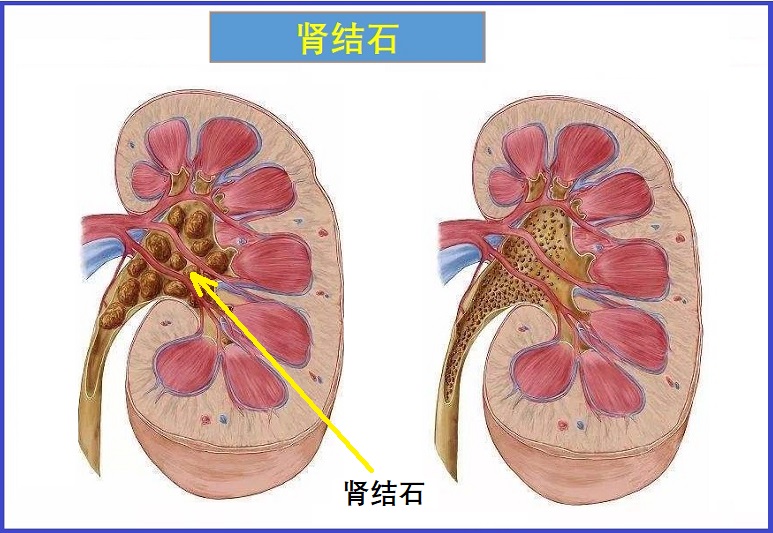
肾结石是一些如石头或结晶样的物质,这些结石形成于肾脏或尿道的一些部位。肾脏清除体内废物,及过滤血液中的盐,以维持血液中的水和电解质平衡。肾结石的主要类型包括草酸钙、磷酸钙
英文名称:Kidney Stones,Renal Colic,Nephrolithiasis,Renal Calculi
定义
肾结石是一些如石头或结晶样的物质,这些结石形成于肾脏或尿道的一些部位。肾脏清除体内废物,及过滤血液中的盐,以维持血液中的水和电解质平衡。肾结石的主要类型包括草酸钙、磷酸钙和尿酸等。病因
肾结石的病因可能取决于结石类型。钙结石是最常见的类型。- 草酸钙或磷酸钙:肾结石主要类型,约占76%。由于尿液中的钙和其他矿物质的浓度太高,或阻止结石形成的其他矿物质太低而引起。
- 尿酸结石:由于尿酸变酸性引起,主要发生在痛风患者身上。
- 鸟粪石:由尿路感染而引起,鸟粪石是由铵盐、镁和磷酸盐组成的,多见于女性。
- 胱氨酸结石:一种罕见的遗传性疾病,导致肾脏中的胱氨酸过量堆积。
风险因素
尿液成分过多的钙、草酸,或过少的钙、尿酸多与肾结石风险相关。可能增加肾结石几率的因素包括:
- 日常饮水不足
- 经常性脱水
- 肾结石家族病史。
- 肾结石个人病史。
- 草酸钙或磷酸钙型结石:
- 饮食中过量的钠和草酸。草酸在绿色、叶状类蔬菜,及巧克力、坚果或茶中都含有。
- 液体摄入不足,尤其是在夏天。
- 甲状旁腺过度活跃。
- 慢性肠道疾病,如炎症性肠炎。
- 某些利尿剂。
- 含钙的抗酸剂。
- 鸟粪石型结石:
- 泌尿系统感染史。
- 在女性中更为常见。
- 尿酸型结石:
- 过量摄入红色肉类、家禽肉。
- 痛风。
症状
在许多人中,肾结石不会引起症状。而其他人可能有症状,包括:
- 尖锐的刺痛,可持续20分钟到一个小时。
- 下腹疼痛,包括腹股沟或生殖器。
- 恶心和呕吐。
- 血尿。
- 尿频。
- 排尿时烧灼痛。
- 发烧。
疗法
治疗取决于肾结石的大小和位置。综合选项可以包括如下:
调整饮食和生活方式
- 橙汁、柠檬汁有助于降低结石。
- 饮食不宜盐分太高、或太甜(高糖分)。
- 不要吃太多的动物肉类。
- 健康、均衡饮食。
- 经常运动、锻炼。
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控肾结石的营养和草本补充剂,主要包括如下:
1. 镁:
镁通过多种机制对草酸钙结石形成风险产生积极影响。镁与消化道中的草酸盐结合,并抑制尿液中草酸钙晶体的形成1,2。较高的镁摄入量与较低的肾结石风险显著相关3,4。
一项针对45,000多名美国男性健康专业人员的研究发现,镁摄入量最高的五分之一的人患肾结石的风险降低29%5。另一项针对311名肾结石患者的研究评估了尿液中的镁水平,这是膳食镁摄入量的已知标志。在该人群中,较高的尿镁与较低的尿草酸显著相关6。
在肾结石的情况下,摄入镁补充剂的时间可能很重要。镁必须与含草酸盐的食物同时存在于消化道中,以结合饮食中的草酸盐并防止其被吸收到总循环中,然后草酸盐必须经过肾脏过滤,并排泄到尿液中。在一项针对六名健康志愿者的临床研究中,研究人员注意到,镁补充剂与草酸盐一起服用会降低草酸盐的吸收,而在草酸盐服用12小时后服用镁补充剂则没有这种效果4。
2. 钙:
研究表明,低钙饮食与草酸钙结石的高风险相关7。另一方面,高膳食钙,即使伴随着草酸盐摄入量的大幅增加,也已被证明可以降低而不是增加肾结石风险8,9,5。这被认为是由于钙能够在肠道中结合膳食草酸盐,从而阻止草酸盐吸收到血液中,最终进入肾脏和尿液10。通过饮食和补充摄入足够的钙与更高的骨密度有关11。这可能是另一种摄入充足钙有助于预防肾结石的方法。随着骨密度的降低,尿钙含量和结石风险增加12。骨吸收或骨分解,会导致钙渗入血液,最终渗入尿液,增加患结石的风险。充足的钙摄入可以减少骨吸收,从而对肾结石提供保护13-15。
在一项对45,000多名没有肾结石的男性健康专业人员进行长达14年随访的研究中,与钙摄入量最少的五分之一相比,60岁以下饮食中钙摄入量最高的男性患肾结石的风险低31%5。另一项针对78,000多名没有肾结石疾病的女性的研究发现,较高的膳食钙与肾结石风险降低5-28%有关,而一项针对96,000多名没有肾结石的年轻女性的研究发现,与饮食中钙摄入量最低的五分之一的女性相比,钙摄入量最高的女性患肾结石的风险低27%9,16。
钙补充剂可以改善尿液化学参数,降低肾结石风险,即使是那些低草酸饮食的人。一项针对32名没有肾结石病史的健康年轻男性的研究发现,补充钙与低草酸饮食相结合,可以降低尿草酸17。
一般建议,钙补充剂应随餐服用,以结合最大量的膳食草酸盐18,19。
3. 矿物柠檬酸盐:
最常见的肾结石类型—草酸钙和尿酸,往往在酸性尿液中形成,最不常见的胱氨酸结石形成也发生在酸性尿液中20。柠檬酸盐通过碱化尿液、结合肠道和尿液中的钙以及抑制草酸钙结晶来预防这些类型的结石21-23。因此在这些类型的结石患者中,低尿柠檬酸盐是一种常见的发现也就不奇怪24。矿物柠檬酸盐,包括钙、镁和钾,在临床实践和研究中用于增加尿柠檬酸盐、碱化尿液,并降低结石形成的速度24-26。
镁、钾和柠檬酸钙。镁和柠檬酸盐都能抑制草酸钙晶体的形成,尽管两者的结合可能比单独使用更有效27。
在一项针对64名有草酸钙肾结石病史的患者的随机对照试验中,与安慰剂相比,三年补充柠檬酸钾镁(提供约255mg镁)可使肾结石风险降低85%28。在一项双盲安慰剂对照试验中,20名参与者卧床休息5周(以增加尿钙排泄量),补充柠檬酸钾镁有效地碱化了尿液,增加了尿液中柠檬酸盐的浓度,降低了尿液中尿酸的浓度,并降低了草酸钙结晶的潜力29。
使用几种不同的钾和镁矿物制剂的研究发现,与不使用镁的治疗相比,在柠檬酸钾治疗中添加镁补充剂,或使用柠檬酸钾镁,在改善尿液化学方面产生了更好的结果30,31。
柠檬酸钾在医学上用于碱化尿液,增加尿液柠檬酸盐,抑制草酸钙和磷酸钙晶体的聚集,并降低肾结石的风险32-34。
用于预防肾结石的柠檬酸钾剂量通常为每天1200–2400mg,这是一种经常导致消化不良的处方强度剂量,使一些人无法忍受33。柠檬酸钾膳食补充剂通常每粒含钾量不超过99mg。与镁或钙形式的柠檬酸盐相比,柠檬酸钾是尿液碱化柠檬酸盐浓度较低的来源35。
一项使用含有柠檬酸钙和柠檬酸钾的补充剂的研究通过降低胃旁路手术患者的酸度和增加尿液柠檬酸盐来改善尿液化学。研究人员得出结论,柠檬酸钙钾可能有助于降低该人群的肾结石风险34。
4. 维生素B6:
维生素B6缺乏部分原因可能是高蛋白饮食。在实验动物和人类中,发现维生素B6不足会增加尿草酸和肾结石风险,补充维生素B6已成功降低高草酸尿36-38。在一项14年对85,557名女性的研究中 ,每天从饮食和补充剂中摄入维生素B6最多的女性患肾结石的风险比摄入最少的女性低34%39。在一项研究中,149名复发性肾结石患者接受了为期4.5-6年的每日三次100mg氧化镁加10mg维生素B6的治疗。在治疗期间,复发率从平均每年1.3下降到每年0.1,降低了92%40。
5. N-乙酰半胱氨酸(NAC):
NAC是抗氧化剂并作为体内主要抗氧化剂谷胱甘肽合成前体41,42。一项具有独立实验室、临床前和临床成分的研究发现,所有三条证据都表明NAC有可能防止草酸钙晶体和肾结石的形成。在该试验的临床阶段,17名草酸钙肾结石患者接受了每天3000mg NAC的治疗。经过一周的治疗,大的尿草酸钙晶体数量减少了60%,三个人经历了结石的自发通过43。
实验室和动物研究的结果提供了额外的证据,证明NAC可以减少草酸钙结晶,并保护肾细胞免受草酸钙的破坏作用44-46。NAC还证明了通过多种机制有助于提高胰岛素敏感性和预防2型糖尿病的活性47。由于胰岛素抵抗似乎与肾结石风险有关48,49,NAC有望成为预防肾结石的综合策略。
6.益生菌:
胃肠道的细菌群组可能在草酸盐分解和代谢中很关键,从而在预防肾结石方面发挥重要作用50,51。
包括乳酸杆菌和双歧杆菌在内的几个属的益生菌似乎能够代谢草酸盐,从而减少尿中的草酸盐并降低肾结石的风险。在一项非对照试验中,六名患有草酸钙肾结石和尿草酸浓度高的患者服用了含有乳酸杆菌和双歧杆菌菌株的补充剂四周。研究结束时,尿草酸浓度下降了近一半52。在随后对10名肠道草酸吸收过度(由几种不同的医疗条件引起)的患者进行的试验中,这些患者服用了含有乳酸杆菌和双歧杆菌菌株的益生菌配方。在每天85亿个细菌的剂量下,一个月后尿草酸的平均含量下降了19%;在第二个月,每天两次的草酸排泄量减少了24%53。然而,后来使用相同益生菌配方的试验无法证明同样的有益效果54,55。
另一项初步试验检测了含有几种双歧杆菌和乳酸杆菌菌株的益生菌补充剂对11名健康人的影响。补充益生菌四周后,草酸盐吸收减少,这一影响主要归因于研究开始时在高草酸盐吸收者中观察到的显著减少56。另一项针对14名没有高草酸尿的结石形成个体的研究在两周内每天饭后三次服用益生菌补充剂,同时进行高草酸饮食。一半的受试者经历了尿草酸减少;减少最多的是在高草酸饮食期间尿草酸增加最多的两个人57。
对不同菌株的实验室研究发现,与双歧杆菌相比,乳酸杆菌表现出更大的草酸降解能力58。
7.鱼油:
一些研究发现,补充鱼油(EPA和DHA)可以通过降低尿钙来降低肾结石的风险。在一项研究中,有肾结石病史的人接受了每天1800 mg EPA的短期(三个月)和长期(18个月)治疗。尿钙浓度在高尿钙人群中下降,但在尿钙正常人群中没有下降59。在另一项研究中,15名健康人每天服用900mg EPA和600mg DHA,持续30天;试验结束时,过量的尿草酸排泄和草酸钙饱和度降低60。这些研究表明鱼油可能在草酸钙肾结石预防中发挥作用。
8. 维生素E:
维生素E保护细胞和血液中的脂质分子免受氧化损伤和应激61,62。在一项实验室研究中,维生素E保护动物肾细胞免受高草酸条件下的氧化损伤,这表明它可能在防止晶体沉积和结石形成方面发挥作用。本研究中发现的维生素E的保护作用通过添加抗氧化剂维生素C而增强63。动物研究发现,维生素E通过减少草酸钙结晶、抑制肾小管细胞中的晶体沉积和保护肾细胞免受氧化损伤来抑制结石的形成64,65。
9. 绿茶:
绿茶和绿茶提取物富含茶多酚植物化学物质,已被证明可以抑制草酸钙结石的形成66-68。在一项动物研究中,对黄酮类儿茶素和表儿茶素调节肾结石生化危险因素的能力进行了评估。与未接受治疗的大鼠相比,接受儿茶素或表儿茶素治疗的大白鼠肾钙含量较低,肾脏中沉积的晶体较少。该研究的作者认为,黄酮类化合物可能保护肾脏内部免受可能引发结石形成的氧化损伤69。
另一项利用实验室和啮齿类动物模型成分的研究调查了儿茶素对草酸钙介导的肾损伤的影响。在实验室环境中,儿茶素保护肾细胞免受草酸钙通常诱导的氧化应激。在该研究的动物成分中,儿茶素似乎可以保护大鼠免受草酸钙的氧化作用70。
10. 槲皮素:
槲皮素对肾结石形成的保护作用已在实验室和临床前模型中进行了研究。一项动物试验将槲皮素和相关分子金丝桃苷的混合物与柠檬酸钾治疗草酸结石进行了比较。与柠檬酸钾相比,槲皮素-金丝桃苷混合物减少了肾组织中的晶体沉积量,并提高了抗氧化酶活性71。在另一项同时使用动物和实验室成分的研究中,槲皮素在两种环境中都能防止草酸盐诱导的损伤,并能防止大鼠肾脏中草酸钙晶体的形成72。
11. 珍珠草:在美洲,珍珠草因利于肾结石而被称为“碎石草(Stonebreaker)”,至今仍然受到自然疗法者认可和使用。一项系统荟萃表明,珍珠草(Phyllanthus niruri,又称叶下珠)可能有效分解肾结石73 。一项随机、前瞻性、长期的研究发现,珍珠草可改善肾结石体外冲击波碎石术后的总体临床结果,且安全没有副作用74 。
12. 六磷酸肌醇(IP-6):又称植酸,组成植物种子、豆类、坚果和全谷物的重要成分。体外和动物研究表明,IP-6作为一种尿液结晶抑制剂,可能防止结石形成75,76。
更多内容可点击其个性化的综合干预方案如下:
以及参阅本网如下专文的有关内容:
医疗干预
一般治疗包括如下:
- 药物治疗如:
- 服用止痛药
- 处方药,帮助在尿液中排出结石。
- 手术治疗:如果结石很大,或引起出血、损伤肾,或引起感染,或影响排尿等,则需要手术。
其他疗法
对于小的肾结石,每天至少喝2-3升的饮水,有助于在尿液中排出。采集一些这种尿液,以便化验分析具体类型和病因。如果很难喝下足够液体或排尿,可能需要住院接受静脉输液。
预防
肾结石一旦形成,就有可能形成更多更大结石。以下方法有助于预防:
- 每天喝足饮水,尤其夏天。
- 咨询医生合适的饮食。
- 根据肾结石类型,可能必须避免某些食物或饮料。
- 根据肾结石类型,某些药物可用于防止结石复发。
参考文献:
1. Kohri K et al. The role of magnesium in calcium oxalate urolithiasis. Br J Urol. Feb 1988;61(2):107-115.
2. Massey L. Magnesium therapy for nephrolithiasis. Magnes Res. 2005;18(2):123-6.
3. Negri AL et al. [Diet in the treatment of renal lithiasis. Pathophysiological basis]. Medicina (B Aires). 2013;73(3):267-271.
4. Zimmermann DJ et al. Importance of magnesium in absorption and excretion of oxalate. Urol Int. 2005;74(3):262-267.
5. Taylor EN et al. Dietary factors and the risk of incident kidney stones in men: new insights after 14 years of follow-up. Journal of the American Society of Nephrology. Dec 2004;15(12):3225-3232.
6. Eisner BH et al. High dietary magnesium intake decreases hyperoxaluria in patients with nephrolithiasis. Urology. Oct 2012;80(4):780-783.
7. Xu H et al. Kidney stones: an update on current pharmacological management and future directions. Expert opinion on pharmacotherapy. Mar 2013;14(4):435-447.
8. Hess B et al. High-calcium intake abolishes hyperoxaluria and reduces urinary crystallization during a 20-fold normal oxalate load in humans. Nephrology, dialysis, transplantation:European Renal Association. Sep 1998;13(9):2241-2247.
9. Sorensen MD et al. Impact of nutritional factors on incident kidney stone formation: a report from the WHI OS. J Urol. May 2012;187(5):1645-1649.
10. Nazzal L et al. Enteric hyperoxaluria: an important cause of end-stage kidney disease. Nephrology, dialysis, transplantation:European Renal Association. 2016 Mar;31(3):375-82.
11. Napoli N et al. Effects of dietary calcium compared with calcium supplements on estrogen metabolism and bone mineral density. The American journal of clinical nutrition. May 2007;85(5):1428-1433.
12. Arrabal-Polo MA et al. Calcium renal lithiasis and bone mineral density. Importance of bone metabolism in urinary lithiasis. Actas Urol Esp. Jun 2013;37(6):362-367.
13. Ettinger AS et al. Effect of calcium supplementation on bone resorption in pregnancy and the early postpartum: a randomized controlled trial in Mexican women. Nutrition journal. 2014;13(1):116.
14. Heaney RP. Calcium supplementation and incident kidney stone risk: a systematic review. Journal of the American College of Nutrition. Oct 2008;27(5):519-527.
15. Martini LA et al. Stop dietary calcium restriction in kidney stone-forming patients. Nutrition reviews. Jul 2002;60(7 Pt 1):212-214.
16. Curhan GC et al. Dietary factors and the risk of incident kidney stones in younger women: Nurses' Health Study II. Archives of internal medicine. Apr 26 2004;164(8):885-891.
17. Stitchantrakul W et al. Effects of calcium supplements on the risk of renal stone formation in a population with low oxalate intake. Southeast Asian J Trop Med Public Health. Dec 2004;35(4):1028-1033.
18. Domrongkitchaiporn S et al. Schedule of taking calcium supplement and the risk of nephrolithiasis. Kidney international. May 2004;65(5):1835-1841.
19. Heilberg IP et al. Optimum nutrition for kidney stone disease. Advances in chronic kidney disease. Mar 2013;20(2):165-174.
20. Frassetto L et al. Treatment and prevention of kidney stones: an update. American family physician. Dec 1 2011;84(11):1234-1242.
21. Goldberg H et al. Urine citrate and renal stone disease. CMAJ : Canadian Medical Association journal. Aug 1989;141(3):217-221.
22. Nicar MJ et al. Inhibition by citrate of spontaneous precipitation of calcium oxalate in vitro. Journal of bone and mineral research. Jun 1987;2(3):215-220.
23. Krieger NS et al. Effect of Potassium Citrate on Calcium Phosphate Stones in a Model of Hypercalciuria. Journal of the American Society of Nephrology. 2015 Dec;26(12):3001-8.
24. Caudarella R et al. Urinary citrate and renal stone disease: the preventive role of alkali citrate treatment. Archivio italiano di urologia, andrologia. Sep 2009;81(3):182-187.
25. Del Valle EE et al. [Citrate and renal stones]. Medicina (B Aires). 2013;73(4):363-368.
26. Sakhaee K et al. Stone forming risk of calcium citrate supplementation in healthy postmenopausal women. The Journal of urology. Sep 2004;172(3):958-961.
27. Rodgers A. Aspects of calcium oxalate crystallization: theory, in vitro studies, and in vivo implementation. Journal of the American Society of Nephrology : JASN. Nov 1999;10 Suppl 14:S351-354.
28. Ettinger B et al. Potassium-magnesium citrate is an effective prophylaxis against recurrent calcium oxalate nephrolithiasis. J Urol. Dec 1997;158(6):2069-2073.
29. Zerwekh JE et al. Reduction of renal stone risk by potassium-magnesium citrate during 5 weeks of bed rest. J Urol. Jun 2007;177(6):2179-2184.
30. Jaipakdee S et al. The effects of potassium and magnesium supplementations on urinary risk factors of renal stone patients. Journal of the Medical Association of Thailand. Mar 2004;87(3):255-263.
31. Kato Y et al. Changes in urinary parameters after oral administration of potassium-sodium citrate and magnesium oxide to prevent urolithiasis. Urology. Jan 2004;63(1):7-11; discussion 11-12.
32. Arrabal-Polo MA et al. Calcium renal lithiasis: metabolic diagnosis and medical treatment. Sao Paulo medical journal. 2013;131(1):46-53.
33. Xu H et al. Kidney stones: an update on current pharmacological management and future directions. Expert opinion on pharmacotherapy. Mar 2013;14(4):435-447.
34. Sakhaee K et al. Biochemical control of bone loss and stone-forming propensity by potassium-calcium citrate after bariatric surgery. Surg Obes Relat Dis. Jan-Feb 2012;8(1):67-72.
35. Higdon J. Linus Pauling Institute. Micronutrient Information Center. Potassium. http://lpi.oregonstate.edu/mic/minerals/potassium. Last updated 12/2010.
36. Murthy MS et al. Effect of pyridoxine supplementation on recurrent stone formers. Int J Clin Pharmacol Ther Toxicol. Sep 1982;20(9):434-437.
37. Nath R et al. Role of Pyridoxine in Oxalate Metabolism. Annals of the New York Academy of Sciences. 1990;585(1):274-284.
38. Kim YN et al. Evaluation of vitamin B6 intake and status of 20- to 64-year-old Koreans. Nutrition research and practice. Dec 2014;8(6):688-694.
39. Curhan GC et al. Intake of vitamins B6 and C and the risk of kidney stones in women. Journal of the American Society of Nephrology. Apr 1999;10(4):840-845.
40. Prien EL et al. Magnesium oxide-pyridoxine therapy for recurrent calcium oxalate calculi. J Urol. Oct 1974;112(4):509-512.
41. Zhang F et al. The cytoprotective effect of N-acetyl-L-cysteine against ROS-induced cytotoxicity is independent of its ability to enhance glutathione synthesis. Toxicological sciences. Mar 2011;120(1):87-97.
42. Rushworth GF et al. Existing and potential therapeutic uses for N-acetylcysteine: the need for conversion to intracellular glutathione for antioxidant benefits. Pharmacology & therapeutics. Feb 2014;141(2):150-159.
43. Fan J et al. The role of Tamm-Horsfall mucoprotein in calcium oxalate crystallization. N-acetylcysteine--a new therapy for calcium oxalate urolithiasis. Br J Urol. Sep 1994;74(3):288-293.
44. Bijarnia RK et al. Modulatory effects of N-acetylcysteine on hyperoxaluric manifestations in rat kidney. Food and chemical toxicology. Jun 2008;46(6):2274-2278.
45. Fishman AI et al. Preventive effect of specific antioxidant on oxidative renal cell injury associated with renal crystal formation. Urology. Aug 2013;82(2):489 e481-487.
46. Davalos M et al. Oxidative renal cell injury induced by calcium oxalate crystal and renoprotection with antioxidants: a possible role of oxidative stress in nephrolithiasis. Journal of endourology / Endourological Society. Mar 2010;24(3):339-345.
47. Lasram MM et al. A review on the possible molecular mechanism of action of N-acetylcysteine against insulin resistance and type-2 diabetes development. Clin Biochem. Apr 25 2015.
48. Assimos DG. Vitamin C supplementation and urinary oxalate excretion. Reviews in urology. Summer 2004;6(3):167.
49. Wong YV et al. The association of metabolic syndrome and urolithiasis. International journal of endocrinology. 2015;2015:570674.
50. Miller AW et al. The metabolic and ecological interactions of oxalate-degrading bacteria in the Mammalian gut. Pathogens. 2013;2(4):636-652.
51. Murphy C et al. Metabolic activity of probiotics-oxalate degradation. Vet Microbiol. Apr 14 2009;136(1-2):100-107.
52. Campieri C et al. Reduction of oxaluria after an oral course of lactic acid bacteria at high concentration. Kidney international. Sep 2001;60(3):1097-1105.
53. Lieske JC et al. Use of a probiotic to decrease enteric hyperoxaluria. Kidney international. Sep 2005;68(3):1244-1249.
54. Lieske JC et al. Diet, but not oral probiotics, effectively reduces urinary oxalate excretion and calcium oxalate supersaturation. Kidney international. Dec 2010;78(11):1178-1185.
55. Goldfarb DS et al. A randomized, controlled trial of lactic acid bacteria for idiopathic hyperoxaluria. Clinical journal of the American Society of Nephrology : CJASN. Jul 2007;2(4):745-749.
56. Okombo J et al. Probiotic-induced reduction of gastrointestinal oxalate absorption in healthy subjects. Urological research. Jun 2010;38(3):169-178.
57. Ferraz RR et al. Effects of Lactobacillus casei and Bifidobacterium breve on urinary oxalate excretion in nephrolithiasis patients. Urological research. Apr 2009;37(2):95-100.
58. Mogna L et al. Screening of different probiotic strains for their in vitro ability to metabolise oxalates: any prospective use in humans? Journal of clinical gastroenterology. Nov-Dec 2014;48 Suppl 1:S91-95.
59. Yasui T et al. Effects of eicosapentaenoic acid on urinary calcium excretion in calcium stone formers. European urology. May 2001;39(5):580-585.
60. Siener R et al. Effect of n-3 fatty acid supplementation on urinary risk factors for calcium oxalate stone formation. J Urol. Feb 2011;185(2):719-724.
61. Princen HM et al. Supplementation with low doses of vitamin E protects LDL from lipid peroxidation in men and women. Arteriosclerosis, thrombosis, and vascular biology. Mar 1995;15(3):325-333.
62. Ni Y et al. Vitamin E protects against lipid peroxidation and rescues tumorigenic phenotypes in cowden/cowden-like patient-derived lymphoblast cells with germline SDHx variants. Clinical cancer research. Sep 15 2012;18(18):4954-4961.
63. Thamilselvan V et al. Oxalate at physiological urine concentrations induces oxidative injury in renal epithelial cells: effect of alpha-tocopherol and ascorbic acid. BJU Int. Jul 2014;114(1):140-150.
64. Huang HS et al. Vitamin E attenuates crystal formation in rat kidneys: roles of renal tubular cell death and crystallization inhibitors. Kidney international. Aug 2006;70(4):699-710.
65. Thamilselvan S et al. Vitamin E therapy prevents hyperoxaluria-induced calcium oxalate crystal deposition in the kidney by improving renal tissue antioxidant status. BJU Int. Jul 2005;96(1):117-126.
66. Jeong BC et al. Effects of green tea on urinary stone formation: an in vivo and in vitro study. Journal of endourology / Endourological Society. May 2006;20(5):356-361.
67. Itoh Y et al. Preventive effects of green tea on renal stone formation and the role of oxidative stress in nephrolithiasis. J Urol. Jan 2005;173(1):271-275.
68. Graham HN. Green tea composition, consumption, and polyphenol chemistry. Preventive Medicine. 5// 1992;21(3):334-350.
69. Grases F et al. Phytotherapy and renal stones: the role of antioxidants. A pilot study in Wistar rats. Urological research. Feb 2009;37(1):35-40.
70. Zhai W et al. Catechin prevents the calcium oxalate monohydrate induced renal calcium crystallization in NRK-52E cells and the ethylene glycol induced renal stone formation in rat. BMC complementary and alternative medicine. 2013;13:228.
71. Zhu W et al. Prophylactic effects of quercetin and hyperoside in a calcium oxalate stone forming rat model. Urolithiasis. Dec 2014;42(6):519-526.
72. Park HK et al. Reduction of oxidative stress in cultured renal tubular cells and preventive effects on renal stone formation by the bioflavonoid quercetin. J Urol. Apr 2008;179(4):1620-1626.
73. Dhawan S et al. Phyllanthus niruri (stone breaker) herbal therapy for kidney stones; a systematic review and meta-analysis of clinical efficacy, and Google Trends analysis of public interest. Can J Urol. 2020 Apr;27(2):10162-10166.
74. Micali S et al. Can Phyllanthus niruri affect the efficacy of extracorporeal shock wave lithotripsy for renal stones? A randomized, prospective, long-term study. J Urol. 2006 Sep;176(3):1020-2.
75. Grases F et al. Inositol hexakisphosphate in urine: the relationship between oral intake and urinary excretion. BJU Int. 2000 Jan;85(1):138-42.
76. Grases F et al. Key Aspects of Myo-Inositol Hexaphosphate (Phytate) and Pathological Calcifications. Molecules. 2019 Dec 4;24(24):4434.
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国国立糖尿病、消化和肾病研究所
http://niddk.nih.gov
美国国立公众健康网
www.medlineplus.gov
美国泌尿护理基金会
http://www.urologyhealth.org
加拿大肾脏健康基金会
http://www.kidney.ca
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

